- ENZYMES VECTORIELLES
- ENZYMES VECTORIELLESENZYMES VECTORIELLESCe sont des enzymes fixées sur les membranes biologiques de manière à permettre, en raison de leur dissymétrie moléculaire, des réactions orientées aboutissant à des transports d’éléments d’un compartiment à l’autre.L’idée de l’existence de telles enzymes résulte de l’évolution convergente de deux concepts.En premier lieu, on avait pensé pendant longtemps que les réactions biochimiques s’effectuaient en phase liquide; les enzymes diffuses dans la solution contractaient une union provisoire avec le substrat et se libéraient une fois le produit formé. Mais ce schéma ne pouvait rendre compte du déroulement des longues chaînes métaboliques, lequel implique une certaine organisation: le rendement de la fermentation alcoolique in vitro, avec seulement du glucose, du phosphate et de la zymase (mélange d’enzymes) n’est guère que de 1 p. 100 par rapport à celui d’une fermentation en présence de levure vivante. En fait, il fut établi que les membranes étaient indispensables aux réactions biochimiques fondamentales et qu’elles portaient les enzymes impliquées dans ces réactions.En second lieu, l’analyse cinétique des transports membranaires actifs a conduit à les considérer comme résultant de l’union provisoire du corps à transporter avec un transporteur protéique, union tout à fait comparable à la formation du complexe enzyme-substrat. Mais la localisation de ces transports au niveau des membranes elles-mêmes, et non au travers de plus larges territoires, a conduit dans la plupart des cas à renoncer à l’idée de transporteurs mobiles et à les supposer fixés sur les membranes.Le premier modèle d’enzyme vectorielle fut proposé par le physiologiste anglais P. Mitchell (1961), ce qui lui valut le prix Nobel en 1978. Il l’imagina pour rendre compte du couplage très fréquent entre une oxydoréduction, qui dégage de l’énergie, et une phosphorylation qui l’incorpore en ATP (théorie chimio-osmotique).Selon Mitchell, l’oxydoréduction AH2 + B = A + BH2 se déroule en deux temps: l’enzyme d’oxydoréduction, vectorielle, incorpore par sa face interne non seulement AH2 et B, mais aussi des protons du compartiment interne, H+; la réaction d’oxydoréduction se produit alors avec passage de deux électrons négatifs de AH2 sur B, lequel capte les H+ présents dans l’enzyme; quant aux H+ libérés à partir de AH2, ils sont non pas rejetés, comme BH2, vers l’intérieur, mais émis à l’extérieur, par suite de la dissymétrie de l’enzyme. Le processus peut donc s’écrire:
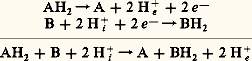 Tout se passe comme s’il y avait eu transport actif de 2 H+ de l’intérieur vers l’extérieur. L’enzyme a fonctionné comme une pompe à protons.Près d’elle, une autre enzyme vectorielle, une ATPase, assurerait la synthèse d’ATP par addition de P4H2, et libération d’eau. Selon Mitchell il ne s’agirait pas d’eau moléculaire mais d’ions H+ émis à l’intérieur et d’ions OH— vers l’extérieur. Les deux systèmes seraient donc couplés et s’entraîneraient l’un l’autre: à l’extérieur, les H+ émis par la pompe à protons s’unissent aux OH— fournis par l’ATPase; à l’intérieur, les H+ émis par l’ATPase sont repris par la pompe.Ce modèle a reçu de nombreuses confirmations expérimentales, et l’on attribue de plus en plus d’importance aux enzymes vectorielles dans les transports actifs transmembranaires et les couplages énergétiques, même si l’on ignore assez souvent le détail des mécanismes en jeu.
Tout se passe comme s’il y avait eu transport actif de 2 H+ de l’intérieur vers l’extérieur. L’enzyme a fonctionné comme une pompe à protons.Près d’elle, une autre enzyme vectorielle, une ATPase, assurerait la synthèse d’ATP par addition de P4H2, et libération d’eau. Selon Mitchell il ne s’agirait pas d’eau moléculaire mais d’ions H+ émis à l’intérieur et d’ions OH— vers l’extérieur. Les deux systèmes seraient donc couplés et s’entraîneraient l’un l’autre: à l’extérieur, les H+ émis par la pompe à protons s’unissent aux OH— fournis par l’ATPase; à l’intérieur, les H+ émis par l’ATPase sont repris par la pompe.Ce modèle a reçu de nombreuses confirmations expérimentales, et l’on attribue de plus en plus d’importance aux enzymes vectorielles dans les transports actifs transmembranaires et les couplages énergétiques, même si l’on ignore assez souvent le détail des mécanismes en jeu.
Encyclopédie Universelle. 2012.
